
Secciones
Servicios
Destacamos


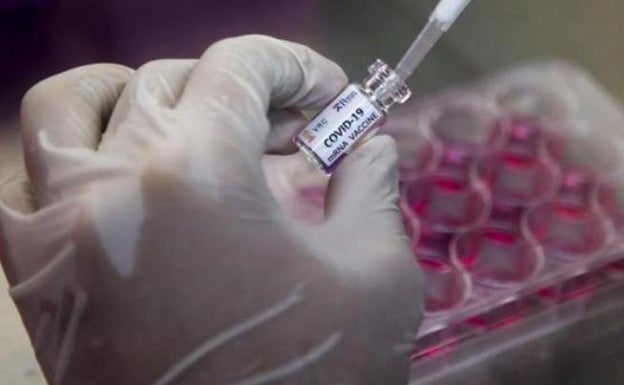
La Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) ha autorizado el ensayo clínico fase III en España de la vacuna contra la Covid-19 de la compañía Janssen, perteneciente a Johnson&Johnson, en ocho centros sanitarios de Madrid, Barcelona y Pamplona.
Se trata del primer ensayo en fase III en la carrera para encontrar una vacuna contra el Covid-19 autorizado en España y que incluirá hasta 30.000 voluntarios procedentes de nueve países: Bélgica, Colombia, Francia, Alemania, Filipinas, Sudáfrica, España, Reino Unido y Estados Unidos.
Este estudio internacional empezará «no antes de diciembre», según fuentes de la compañía, y lo hará con la selección de los voluntarios: entre 2.000 y 3.000 en España. En principio, no hay un «cupo» cerrado para cada estado. El reclutamiento es competitivo, lo que significa que, según cada centro vaya inscribiendo participantes, se irán restando plazas de ese total de 30.000 personas.
En la autorización de la Aemps figuran ocho centros en España de Madrid, Barcelona y Pamplona. Son la Clínica Universitaria de Navarra (Pamplona); el Hospital Clinic de Barcelona; el Hospital Quironsalud de Barcelona; el Hospital Universitario Germans Trias i Pujol de Badalona (Barcelona); el Hospital Universitario Vall D'Hebron (Barcelona); el Hospital Universitario de la Princesa (Madrid); el Hospital Universitario La Paz (Madrid) y el Hospital Universitario QuironSalud de Madrid.
Se buscan participantes entre 18 y 60 años de edad por un lado, y mayores de 60 por otro. Un 20% de los pacientes serán menores de 40 años, y un 30% mayores de 60 años. El participante debe presentar un estado de salud bueno o estable, y tener un IMC menor de 30 kg/m2.
En una primera etapa del ensayo, se vacunará a aquellas personas que no tengan enfermedades que puedan agravar la evolución del Covid (como obesidad), pero sí que pueden tener enfermedades subyacentes, siempre que sus síntomas y signos se mantengan estables y bien controlados. Si los participantes reciben medicación para una afección, la dosis de la medicación debe haber permanecido estable durante al menos 12 semanas.
Además, en una segunda etapa del mismo estudio, el participante puede presentar enfermedades con riesgo de agravar el Covid, pero siempre que esté estable y bien controlada (por ejemplo, sería el caso de una infección por VIH estable/bien controlada). Si los participantes reciben medicación a una enfermedad concomitante, la dosis de la medicación debe haber permanecido estable durante al menos 12 semanas antes de la primera vacunación y se debe prever que se mantenga estable durante todo el estudio.
Los motivos por los que se excluyen a posibles candidatos incluyen tener alergias conocidas o antecedentes de anafilaxia; haber recibido un fármaco en investigación o presentar una función anómala del sistema inmunitario por enfermedades autoinmunes o una enfermedad renal crónica que requiera de diálisis. Sin embargo, los participantes con afecciones clínicas estables en tratamiento no inmunomodulador (por ejemplo, tiroiditis autoinmune o enfermedad reumática inflamatoria autoinmune, como artritis reumatoide) pueden inscribirse a criterio del investigador.
A lo largo del ensayo se administrará tanto la vacuna como un placebo y hasta que finalice el ensayo, los voluntarios no sabrán qué les han puesto. No obstante, normalmente a los voluntarios que han recibido placebo se les da prioridad durante la vacunación.
Como cualquier ensayo clínico, se percibirá una compensación económica por los gastos derivados de la participación. En el ensayo de fase 2 de esta misma vacuna, esta compensación no superó los 70 o 80 euros por día.
La legislación europea fija que «en los ensayos clínicos, debe garantizarse una indemnización por daños y perjuicios cuando se solicite con éxito de conformidad con la legislación aplicable. Por consiguiente, los Estados miembros deben velar por que existan mecanismos de indemnización de los daños y perjuicios sufridos por un sujeto de ensayo que sean acordes con la naturaleza y el alcance del riesgo».
¿Ya eres suscriptor/a? Inicia sesión
Publicidad
Publicidad
Te puede interesar
Publicidad
Publicidad
Esta funcionalidad es exclusiva para suscriptores.
Reporta un error en esta noticia
Comentar es una ventaja exclusiva para suscriptores
¿Ya eres suscriptor?
Inicia sesiónNecesitas ser suscriptor para poder votar.