
Secciones
Servicios
Destacamos

SUR
Viernes, 11 de junio 2010, 03:36
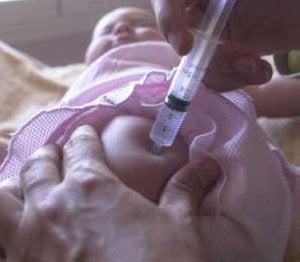
Las agencias europeas de medicamentos están evaluando el hallazgo de ADN de circovirus porcino de los tipos 1 y 2 (PCV-1 y PCV-2) en la vacuna Rotateq, una terapia comercializada en España por Sanofi Pasteur MSA. Aunque no hay ningún dato que sugiera que la presencia de estos fragmentos de ADN supongan un riesgo para la salud, estos no deberían estar en esta vacuna. Por ello, la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS), dependiente del Ministerio de Sanidad, recomienda como medida de precaución y en tanto no se concluya la investigación, no iniciar la vacunación frente a la gastroenteritis por rotavirus con la vacuna Rotateq.
La presencia anómala de este ADN fue descubierta tras estudios realizados como consecuencia de haberse detectado fragmentos de ADN de PCV-1 en la otra vacuna frente a rotavirus (vacuna Rotarix, de la compañía GlaxoSmithKline). Este hallazgo dio lugar a otra nota informativa de la AEMPS para profesionales sanitarios el pasado 29 de marzo.
El fabricante de Rotateq ha confirmado la presencia de pequeñas cantidades de ADN de los virus PCV-1 y PCV-2. Ninguno de los dos causa enfermedad en humanos. Las agencias europeas de medicamentos han evaluado los datos disponibles en la reunión del Comité de Medicamentos Humanos (CHMP) del pasado mes de mayo y han concluido que la presencia de este ADN del virus PCV-1 no representa un problema para la salud humana. Sin embargo, se ha requerido a la compañía Sanofi-Pasteur-MSD que aporte información adicional que se irá evaluando de forma continuada durante las próximas semanas.
Ante estos hechos, y a la espera de concluir el análisis, la AEMPS ha decidido no autorizar la liberación de nuevos lotes de vacuna Rotateq con este defecto de calidad al mercado español. Ello podría conducir en las próximas semanas a un desabastecimiento de esta vacuna en el canal de distribución farmacéutico.
La vacunación para el rotavirus no forma parte del calendario vacunal en España y la AEMPS considera que no hay motivos para utilizar Rotateq en nuestro país en las condiciones actuales, en tanto se esclarecen aquellos aspectos que aun están en discusión y para los que se han pedido aclaraciones a la compañía. Sin embargo, la AEMPS advierte de que este balance beneficio/riesgo puede ser distinto en otros países en los que la gastroenteritis por rotavirus representa un problema de salud más importante y donde los beneficios de la vacuna justifican mantener su utilización mientras prosiguen las evaluaciones.
Recomendaciones
Las recomendaciones de la AEMPS a los profesionales sanitarios en España son informar de que la vacuna frente a rotavirus no forma parte del calendario vacunal español acordado por la Comisión de Salud Pública y no iniciar la vacunación con la vacuna Rotateq. Asimismo, señalan que no es necesario completar el esquema de vacunación de tres dosis para niños que ya han recibido alguna.
Respecto a los pequeños que se hayan vacunado con Rotateq, no hace falta ninguna acción más dado que la eficacia de la vacunación no está en cuestión y no presenta ningún problema de seguridad. No hay ningún dato que sugiera que la vacunación con Rotateq haya podido producir daño alguno, por lo que no es necesario un seguimiento especial. La AEMPS seguirá informando puntualmente del resultado de la evaluación de los nuevos datos que se han solicitado a Sanofi-Pasteur-MSD y de cualquier resolución que, como consecuencia de ello, pueda derivarse.
Publicidad
Publicidad
Te puede interesar
Publicidad
Publicidad
Recomendaciones para ti
Favoritos de los suscriptores
Tiroteo en Málaga con cuatro heridos en Carretera de Cádiz a plena luz del día
María José Díaz Alcalá
Esta funcionalidad es exclusiva para suscriptores.
Reporta un error en esta noticia
Comentar es una ventaja exclusiva para suscriptores
¿Ya eres suscriptor?
Inicia sesiónNecesitas ser suscriptor para poder votar.